第十九節 釩酸銨(Ammonium Vanadate)
概述
釩酸銨,分子式為NH4VO3,分子量等於117.00,是一種白色的晶體,市上所售的為分析純的商品。
釩酸銨的製備
釩酸銨的製備 在釩酐(即五氧化二釩V2O5)的鹼性溶液中,加入氯化銨,使釩酸銨析出沈澱而得。如下式:
V2O5+2NaOH+2NH4Cl→2NH4VO3+2NaCl+H2O
釩酸銨的性質
1.釩酸銨微溶於冷水,但易溶於鹽酸中,並與鹽酸作用,生成多釩酸銨而使溶液成橘黃色。化學反應式如下:
6NH4VO3+2HCl→2NH4Cl+(NH4)4V6O17+H2O
2.在釩酸銨的酸性溶液中(例如鹽酸),加入1~2滴H2O2溶液,生成高釩酸HVO4,溶液呈現櫻桃紅色或帶有玫瑰的褐色(這是釩酸鹽的定性方法)。
NH4VO3+HCl+H2O2→HVO4+NH4Cl+H2O
3.在釩酸銨的鹽酸溶液中,加入還原劑如重亞硫酸鈉NaHSO3,釩酸銨就被還原而生成二氯化釩VCl2,這時溶液顯現2價釩離子V++的紫色。化學反應式
如下:
2NH4VO3+5HCl+3NaHSO3→
2VCl2+NaCl+(NH4)2SO4+2NaHSO4+3H2O
釩酸銨分析法
釩酸銨分析法
碘量法 此法分析的原理是根據釩酸銨為一氧化劑,它在酸性介質中有足量碘化鉀的存在,被I-從5價釩V+5還原成4價釩V+4,而I-則被NH4VO3氧化而使碘游離,這析出的I2再以硫代硫酸鈉標準溶液滴定。反應式如下:
2NH4VO3+2KI+4H2SO4→
2VOSO4+(NH4)2SO4+K2SO4+4H2O+I2
I2+2Na2S2O3→2NaI+Na2S4O6
操作 精確稱取試品0.1克,置於200毫升的錐形燒瓶中,加水30毫升,再慢慢加入98%的濃硫酸10毫升,搖蕩,使完全溶解,待冷後加入碘化鉀1克,緊塞瓶蓋,搖勻片刻,靜置4~5分鐘使作用完全,以0.1N硫代硫酸鈉溶液滴定,滴至黃色即將消失時,加入澱粉溶液數毫升作指示劑,繼以0.1N硫代硫酸鈉溶液滴定,滴至藍色消失時為止。
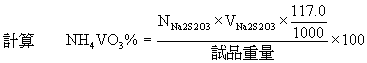
或 1毫升0.1NNa2S2O3=0.0117克NH4VO3

釩酸銨在印染上的用途
釩酸銨在印染上的用途
作印地科素染料直接印花氯酸銨蒸處法中氧化劑 印地科素直接印花除亞硝酸鈉法外,有氯酸銨蒸處法。本法將白布用印地科素色漿印花、烘乾後,經過汽蒸而使染料顯色。
蒸處法是利用酸性鹽在汽蒸時分解為酸質,使染料氧化,因此在汽蒸過程中完成顯色。適用於汽蒸法的化學品很多,一般常用的為氯酸銨法,添加釩酸銨做氧化劑;棉織物經印花後汽蒸,就可發色。釩酸銨的氧化能力很強,易使染料早期氧化調製成的色漿很不穩定,現已較少應用。