第三節 漂白粉(Bleaching Powder)
一、概述
漂白粉學名次氯酸鈣,也稱為次氯酸鈣氯化鈣的複鹽,通稱漂粉,是一 些成分複雜的化合物,在不同比例下組成的。化學成分大致是CaCl2‧Ca OH)2及Ca(OCl)2 ‧2Ca(OH)2;但為了簡便起見,一般都用來代表它的分子式,分子量126.994。
1漂白粉的製備
漂白粉的製造由氯作用於消石灰製成。如下式:

2漂白粉的性狀
規格 一般依其含有效氯的多少,分為三種,甲種含有效氯31~36%, 乙種含有效氯29~31%,丙種含有效氯25~29%。 包裝 鐵桶裝,每桶有120公斤、150公斤等。木箱裝,每箱50公斤。 貯運 切忌露天日光曝曬或雨淋。工作時戴口罩,用大蘇打溶液浸潤後 ,可以脫氯。漂白粉為不穩定化合物,它的有效成份隨存放時間增長而 降低。在夏季六、七、八三個月中損失最大,品質最好的每月損失1% ,中等的損失2%,最多的達3%;春秋雨季每月損失平均為0.3%。因 此不宜久貯,最好立即用去。
3漂白粉的性質
1. 優良的漂白粉不含塊粒,而為白色粉末,外觀與熟石灰相似,具有近 似氯氣的特臭。性毒,吸入人體引起鼻塞、喉痛,重者中毒。
2.漂白粉受高熱會發生爆炸,與有機物、易燃液體混合,能發熱自燃。
3.漂白粉暴露於空氣中,易吸收水分、二氧化碳,分解很快而放出次氯 酸和氯氣。反應式如下:
CaOCl2+H2O+CO2→CaCO3+HCl+HClO
HCl+HClO→H2O+Cl2↑
次氯酸也即分解,生成氯化氫和新生氧:
HClO→HCl+[O]
次氯酸 氯化氫 新生氧
新生氧的氧化能力很強,所以漂白粉是強氧化劑,漂白作用也是由於這新生 氧具有破壞色素團的能力,使有色物質變成無色物質,從而達到漂白效果。 4.漂白粉遇硫酸或鹽酸即分解,並放出次氯酸。次氯酸再行分解,放出新生 氧。新生氧能破壞色素團,達到漂白效果。棉布用漂白粉漂白後,再用硫酸 或鹽酸進行酸洗,可起進一步的漂白作用,即根據此理。反應式如下:
CaOCl2+H2SO4→CaSO4+HCl+HClO
CaOCl2+2HCl→CaCl2+HCl+HClO
HClO→HCl+[O]
5.日光、酸氣及熱量均能使漂白粉徐徐變化,減弱了它有效氯成分,故 需貯盛於密閉桶中,切忌著熱、著濕或著酸氣。
6.漂白粉久置後,雖然不接觸水、空氣或無機酸等,但本身也能逐漸分 解成氯化鈣,並放出氧氣,而降低它的有效成分。反應式如下:
2CaCl(OCl0→2CaCl2+O2↑
7.漂白粉有消毒、殺菌能力。溶解於水,呈鹼性反應。
8.各濃度的漂白粉溶液在15℃下的強度見下面附表。
漂白粉溶液在15℃下的強度
| 波 美 度 °Be' | 每升溶液含 有效氯克數 |
| 0.25 0.4 0.5 0.7 0.8 1.0 1.5 2 3 4 5 6 7 8 9 10 11 12 13 14 15 | 0.96 |
4漂白粉分析法
一般優良的漂白粉含有效氯約30~35%。高度的漂白粉通稱漂粉精,含有效
氯一倍於普通漂白粉。
有效氯的意義 有效氯是指漂白粉的有效成分,即一定量的漂白粉與酸作用後所生成的氯量,用百分率來表示。事實上有效氯是通過氯素化合物在水中所起的氧化反應,根據氧化反應的強度來表示的。漂白粉或漂粉精的分析法 一般採用碘量法來測定漂粉中的有效氯,其法是將一定量的漂白粉,於酸性溶液中與碘化鉀起氧化作用而釋出相當量的碘;再以硫代硫酸鈉標準溶液來滴定碘,然後根據硫代硫酸鈉標準溶液的用量來
計算出漂白粉的有效氯量。
操作1 用稱量瓶精確稱取試品約5克,移置瓷研缽中,加少量的水(約20毫升)研磨成勻和的糊狀,再加水約20毫升攪拌,靜放數分鐘待粗粒沈降,傾出上層清液,經漏斗注入500毫升的量瓶中,研缽中殘留的試品仍加少量水研磨後注入量瓶中。如此重復操作數次,最後將研缽洗淨,亦注入量瓶中,繼加水稀釋至 500毫升刻度,搖勻。用50毫升的單標移液管移取此勻和的試溶液50毫升於300毫升的錐形燒瓶
中,再加水100毫升,漂白粉起水解作用而放出少量的氯:

加10%碘化鉀溶液20毫升,試品即變成淡黃色(少量碘的色澤):
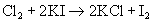
加6N醋酸溶液15毫升(加速漂白粉分解)試液立即變成深黃色(多量碘的色
澤):
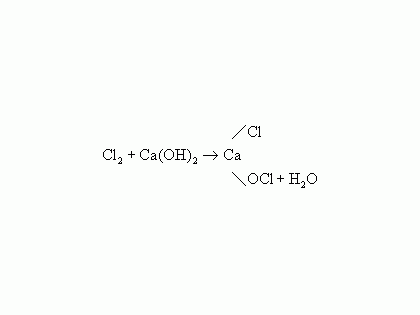
(2)Cl2+2Kl→2KCl+I2
氯 碘化鉀 碘
將0.1N硫代硫酸鈉,由滴管中滴入試液內,愈速愈好,至溶液微呈淡黃色(淡黃色的重現,由於碘量減少的原因),始加澱粉溶液數滴,立現藍色。I2(自由狀態碘)+澱粉→呈藍色續將0.1N硫代硫酸鈉,再由滴管內徐徐放下,直至試液變成無色(由於碘化鈉NaI無色物的生成),即為終點:
I2+2Na2S2O3→Na2S4O6+2NaI
計算
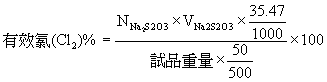
或 1毫升0.1N硫代硫酸鈉=0.003547克有效氯

操作2 移取上述所製的試品溶液50毫升,加入預先放有10%碘化鉀溶液20毫升、水100毫升及6N醋酸溶液15毫升的300毫升錐形燒瓶中,立即用0.1N硫代硫酸鈉溶液滴定釋出的碘I2,在黃色即將消失時加入澱粉溶液3~4毫升,繼續滴定至藍色消失時為止。反應式如下:

Cl2+2KI→2KCl+I2
I2+2Na2S2O3→2NaI+Na2S4O6
計算 同上述操作1.法。
操作3 稱取漂白粉0.5克,置於100毫升燒杯裡,加冷水約3毫升,用玻璃棒將約攪拌成漿狀(要求攪拌均勻,達到沒有一點漂白粉的細小粒子)。再加水50 毫升,攪勻。觀察玻璃燒杯底上,是否留有殘餘的漂白粉粒子,如有,需用玻璃棒端把漂白粉粒子輕輕研觸,使分散(注意,防止把燒杯戳破)。另取300毫升錐形燒瓶一只,加水50毫升,10%碘化鉀溶液20毫升,6N醋酸10毫升,搖勻。把做好的漂白粉溶液傾注到300毫升錐形燒瓶裡(這瓶裡已放有水、碘化鉀、醋酸),立即用0.1N硫代硫酸鈉溶液滴定,滴至淡黃色時,加入澱粉溶液數毫升立呈藍色,繼續用0.1NNa2S2O3滴至藍色消失時即為終點。計算舉例:稱取漂粉試品0.5克,用0.1N硫代硫酸鈉溶液滴定時耗用43毫升,
那麼,這漂白粉裡所含的有效氯是30.53%。計算式如下:


注 操作時應注意下列幾點:
1.KI的用量:碘化鉀的用量要比按反應方程式所需的量多數倍,這樣可以使反應時所生成的幾乎不溶於水的碘I2不會沈澱析出,在有過量的KI存在時,不會發生碘的沈澱現象,這是由於三碘化鉀KI3的存在,碘可溶於碘化鉀溶
液中:
I2+KI
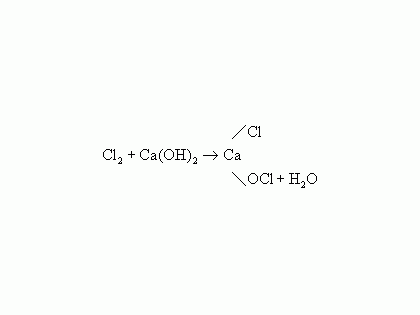
KI3的存在並不妨礙用硫代硫酸鈉來滴定碘。因為由於上述反應的可逆性,這種 KI3的溶液含有大量游離碘I2,以後隨著游離碘在與還原劑硫代硫酸鈉反應時的逐漸消耗,KI3便逐漸分解,於是碘就繼續不斷的進入溶液中。
2.澱粉溶液的加入:用硫代硫酸鈉滴定碘量,必須在滴定將近終點前,當溶液中僅存很少量游離碘I2,即溶液從深褐色變成淡黃色時,再加入澱粉溶液,否則,澱粉吸附了大量的碘後,很慢地將碘放回到溶液中去,因此溶液易被滴過量,以致造成誤差。
3.碘遇澱粉呈藍色的推究:碘遇澱粉反應的本質,一般是以碘與澱粉為主體
所形成的膠質,是一種吸著體,反應的結果呈現突出的藍色。這是極敏銳的反應,能夠檢出2×10-5N的碘,因此具有很大的準確度。可是溫度高或存在有機物時,敏感度就很薄弱。
4.藍色再現的推究:在終點一旦消失的藍色有時再現,其主要原因有三:
(1)酸不足。
(2)有尚未溶解的漂白粉微粒存在,以致反應遲緩。
(3)如果不是很快變藍(經過5~10分鐘),那麼就是由於空氣中的氧化作用所造成。
5漂白粉在印染上的用途
作棉織物漂白劑 棉織物經過鹼液煮練後,使棉上大部分天然雜質,因鹼質的作用而除去,但原棉中仍有殘留色素而現棕黃色。無論何種色素,受氧化作用後,色素的分子立即分裂,變為其它物體,色素因而消失。漂白粉用以漂白棉織物,即借氧化作用,使色素消除。因漂白粉經漂白工程的加水、吃酸等必需步驟,即分解而放出有效氯,這有效氯與水作用而產生新生氧。
如下式:
Cl2+H2O→2HCl+[O]
色素受新生氧的氧化作用,構造破裂,色素因而消滅,且變成可溶物而被水洗去(故氧化劑的漂白品的白度能保持長久)。
注 文獻載稱:1.當漂白粉溶解於水中時,它的分子即成為次氯酸鈣及氯化
鈣:
2Ca(OCl2)→Ca(OCl)2+CaCl2
漂白粉 次氯酸鈣 氯化鈣
2.氯化鈣是不能起漂白作用的,它大部分沈澱在溶解槽底,作為廢物而被清除出去。能起漂白作用的是次氯酸鈣。
3.次氯酸鈣又與水起分解作用,成為氫氧化鈣(即熟石灰)及次氯酸:
Ca(OCl)2+2H2O→Ca(OH)2+2HOCl
次氯酸鈣 水 氫氧化鈣 次氯酸
氫氧化鈣是不能起漂白作用的東西,它大部分又沈澱在溶解槽底,作為廢物而被清除出去。能起漂白作用的是“次氯酸”(HOCl)。
4.次氯酸是很不穩定的東西,它在水中進行著各種不同的反應,我們試舉出
幾個反應來:
(1)2HOCl
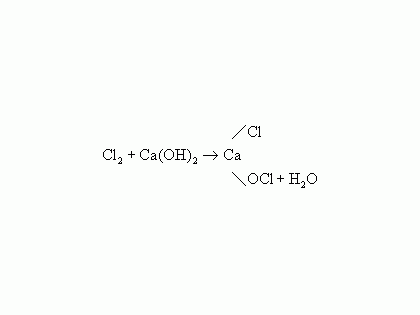
次氯酸 一氧化氯 水
(2)HOCl
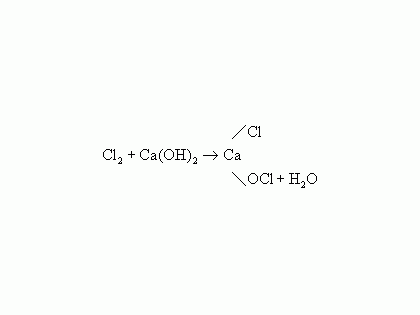
次氯酸 氯化氫 新生態氧
(3)HOCl+HCl→H2O+Cl2
次氯酸 氯化氫 水 氯
5.以上三個反應中所產生的產物,不論其為一氧化氯,或是新生態氧,或是氯,都是很好的氧化劑,都具有氧化作用,換句話說,都能進行漂白。漂白粉的所以能夠漂白,其真正的力量即在於此。天然色素+氧化劑→天然色素被破壞,變成容易被洗去的無色物質
6.我們為什麼只能很籠統地寫成上面這樣呢?因為我們還不了解這些天然色素的構造及其分子式,也不能確說,經過氧化之後,它們最後變成了什麼東西,所以我們就不能寫出平衡的化學方程式來,而只能寫出以上的樣子。
7.漂白粉為什麼是一個氧化劑呢?從電子學說來講,氧化劑一定要獲取電子,進行氧化,但它本身卻被還原,增加了它的負化合價。我們試看漂白粉中
一些具有氧化作用的物質,它們能進行些什麼反應?
8.漂白粉中真正的有效成分是:氯、一氧化氯及新生態氧。
9.氯(Cl2)是在分子狀態中,換句話說,它是電性中和的,它的化合價是“零”。當它與棉纖維上的天然色素發生反應時,它獲取了電子,本身被還原了,同時使天然色素氧化成為無色的易被洗去的氧化物,因此棉纖維上的顏
色就被漂白了。
Cl2(氯分子)+2e(電子)(由天然色素失去)→
2Cl-(氯離子)(增加了負化合價)
10.再如一氧化氯(Cl2O)中的氯,它的化合價是正1,它可以獲取2個電子而成為化合價是負1的氯陰離子:Cl++2e(由天然色素失去)→Cl-(增加了負化合價)Cl+本身被還原了,而天然色素則因失去電子而被氧化了。
11.再如新生態氧[O],因它是在原子狀態,所以非常活潑,能使天然色素氧化成為無色的易被洗去的氧化物。